Kleinstroboter im Körper verfolgen
Forscher am Max-Planck-Institut für Intelligente Systeme in Stuttgart und vom ETH Center for Learning Systems Zürich haben ein Bildgebungsverfahren entwickelt, mit dem zellgroße Mikroroboter erstmals einzeln und hochaufgelöst in einem lebenden Organismus erkannt und verfolgt werden können, in Echtzeit.
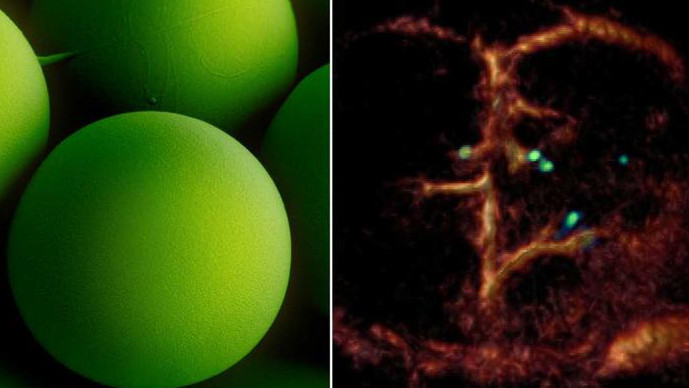
An Mikrorobotern für den Einsatz in der Medizin wird bereits seit längerem gearbeitet. Damit dieser Einsatz Wirklichkeit werden kann, muss es allerdings auch ein Verfahren geben, mit dem die für das menschliche Auge unsichtbaren Mikroroboter von außen durch den menschlichen Körper gesteuert und verfolgt werden können. Außerdem ist es erforderlich zu prüfen, ob sie ihre Aufgaben, zum Beispiel den Medikamententransport an einen bestimmten Ort im Körper, fehlerfrei erfüllen. Die Wissenschaftler des MPI für Intelligente Systeme und von der ETH Zürich erzielten nun einen wichtigen Durchbruch. Dafür kombinierten sie Mikrorobotik und Bildgebung. Es gelang ihnen, mit Hilfe eines nichtinvasiven, bildgebenden Verfahrens bis zu fünf Mikrometer kleine Roboter in den Hirn-Blutgefäßen von Mäusen in Echtzeit nachzuweisen und sie zu verfolgen. Dafür nutzten die Forscher Mikroroboter mit einer Größe von 5 bis 20 Mikrometern. Die kleinsten Roboter sind etwa so groß wie die roten Blutkörperchen, die einen Durchmesser von 7 bis 8 Mikrometern haben. Diese Größe macht es möglich, dass sich die intravenös injizierten Mikroroboter selbst durch die dünnsten Mikrokapillaren im Hirn einer Maus fortbewegen können. Außerdem entwickelten die Forscher eine spezielle optoakustische Tomographietechnik, um die Miniroboter tatsächlich einzeln, hochaufgelöst und in Echtzeit zu erkennen. Dabei wird zunächst Licht ausgesendet, das vom jeweiligen Gewebe absorbiert wird. Dies erzeugt winzige Ultraschallwellen, die man erkennen und analysieren kann, um hochauflösende volumetrische Bilder zu erhalten. So können die winzigen Roboter in tiefen und schwer zugänglichen Regionen des Körpers und des Gehirns aufgespürt werden, was mit optischer Mikroskopie oder einer anderen Bildgebungstechnik nicht möglich gewesen wäre.
Um die Mikroroboter auf den Bildern deutlich sichtbar zu machen, war ein geeignetes Kontrastmittel nötig. Für ihre Studie verwendeten die Forscher deshalb kugelförmige Mikroroboter auf der Basis von Siliziumdioxidpartikeln mit einer sogenannten Janus-Beschichtung. Dieser robuste Roboter-Typ eignet sich sehr gut für anspruchsvolle medizinische Aufgaben. Benannt ist er nach dem römischen Gott Janus, dem zwei Gesichter nachgesagt werden. Bei den Robotern sind die beiden Kugelhälften jeweils unterschiedlich beschichtet – eine Hälfte mit Nickel, die andere mit Gold.
„Gold ist ein sehr gutes Kontrastmittel für die optoakustische Bildgebung“, erklärt Daniel Razansky, Professor für Biomedizinische Bildgebung der ETH Zürich und der Universität Zürich sowie Mitglied des CLS, „ohne die Goldschicht ist das von den Mikrorobotern erzeugte Signal schlicht zu schwach, um erkannt zu werden.“ Zusätzlich wurde der Einsatz kleiner Bläschen, sogenannte Nanoliposomen getestet, die einen fluoreszierenden, grünen Farbstoff enthielten, ebenalls ein Kontrastmittel. „Liposomen haben zudem den Vorteil, dass man sie mit Medikamenten beladen kann, was für künftige Ansätze zur gezielten Verabreichung von Medikamenten wichtig ist“, sagt Paul Wrede, Doktorand und Fellow am Max Planck ETH Center for Learning Systems (CLS) sowie Erstautor der Studie. Die Einsatzmöglichkeiten der Liposomen werden in einer Folgestudie untersucht.
Mit dem Gold lässt sich zudem die zelltoxische Wirkung der Nickelbeschichtung minimieren – schließlich müssen die künftigen Mikroroboter, wenn sie in lebenden Tieren oder Menschen eingesetzt werden sollen, bioverträglich und ungiftig sein, was Teil einer laufenden Forschungsarbeit ist. Und die Wissenschaftler verwendeten Nickel als magnetisches Antriebsmedium zusammen mit einem einfachen Permanentmagneten, um die Roboter zu ziehen. In Folgestudien wollen sie die optoakustische Bildgebung auch mit einer komplexeren Bewegungssteuerung testen, die rotierende Magnetfelder verwendet.
„Das gäbe uns die Möglichkeit, die Mikroroboter auch in stark fließendem Blut präzise zu steuern und zu bewegen“, so Metin Sitti, einem führenden Mikrorobotiker, der als Abteilungsleiter am Max-Planck-Institut für Intelligente Systeme (MPI-IS) und ETH-Professor für Physische Intelligenz ebenfalls CLS-Mitglied ist. „In der vorliegenden Studie haben wir uns darauf konzentriert, die Mikroroboter sichtbar zu machen. Das Projekt war sehr erfolgreich dank der exzellenten Zusammenarbeit am CLS, die es ermöglichte, die Expertise der beiden Forschungsgruppen des MPI-IS in Stuttgart für den Roboterteil und der ETH Zürich für den bildgebenden Teil zu kombinieren“, schließt er. Sittis Forschung wurde 2020 auf der Falling Walls Conference in Berlin zum Durchbruch des Jahres in der Kategorie Engineering & Technology gewählt.
Ihre Forschungsergebnisse veröffentlichten die Wissenschaftler Mitte Mai in ScienceAdvances.

 TH Mannheim/Foto: Michael Ganninger
TH Mannheim/Foto: Michael Ganninger
 Daniel Fuhr - stock.adobe.com
Daniel Fuhr - stock.adobe.com