Pentixapharma sieht bei FDA-Vorgaben klarer
Pentixapharm hat von der FDA das schriftliche Feedback zum Design der geplanten Phase III-PANDA-Studie mit dem Radiodiagnostikum [⁶⁸Ga]Ga-PentixaFor erhalten. Die Behörde sieht keine wesentlichen Bedenken und präzisiert statistische sowie methodische Anforderungen für die Studie bei primärem Aldosteronismus (PA). Ziel ist eine Subtypisierung von Patienten.

 Messe München
Messe München
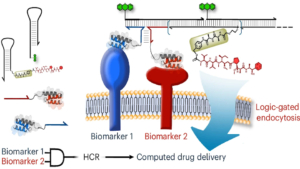 Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0
Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0