Pentixapharm: FDA gibt grünes Licht für CXCR4-Theranostik in der Hämatologie
Die U.S. Food and Drug Administration hat zwei IND-Anträge der Berlin-Würzburger Pentixapharm Holding AG genehmigt und den Start einer klinischen Phase I/II-Studie im CXCR4-basierten Theranostik-Programm („Study May Proceed“) ermöglicht.
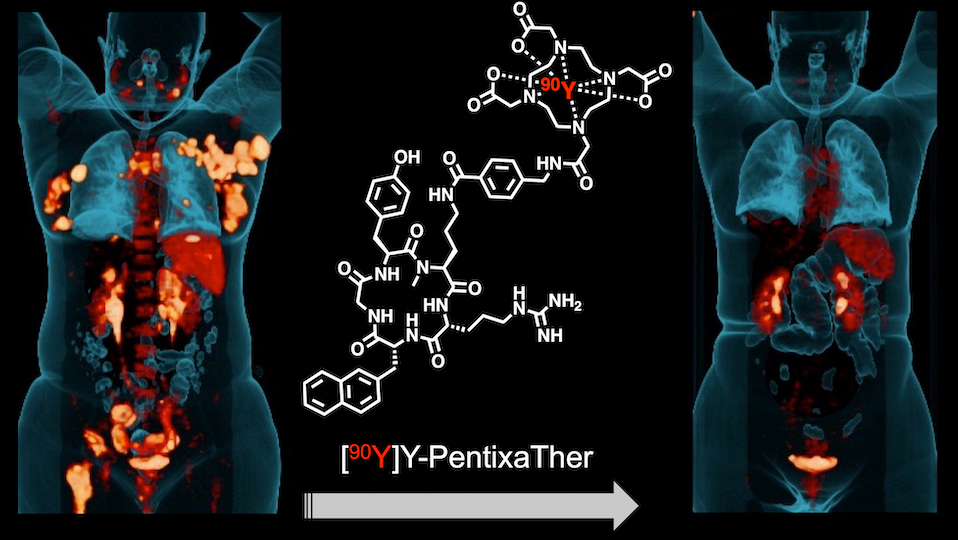
Die FDA hat zwei IND-Anträge der Berliner Pentixapharm Holding AG genehmigt und den Start einer klinischen Phase I/II-Studie im CXCR4-basierten Theranostik-Programm („Study May Proceed“) ermöglicht. Im Zentrum steht das theranostische Paar PentixaFor (Diagnostik) und [90Y]Y-PentixaTher (Therapie), das im Rahmen der Studie PENTHERA zur gezielten Knochenmark-Konditionierung vor Stammzelltransplantationen bei akuter myeloischer Leukämie (AML) und multiplem Myelom (MM) geprüft werden soll.
Theranostik verbindet lokale Diagnostik mit lokaler Therapie
Theranostik – die Kombination aus molekularer Bildgebung und darauf abgestimmter Radionuklidtherapie – gilt als eines der dynamischsten Felder der Onkologie. Während klassische Konditionierungsregime vor einer Transplantation auf hochdosierter Chemotherapie oder Ganzkörperbestrahlung beruhen und entsprechend systemisch toxisch wirken, zielt der CXCR4-gerichtete Ansatz auf eine biologisch präzisere Vorbereitung des Knochenmarks. CXCR4 ist bei verschiedenen hämatologischen Malignomen stark exprimiert und ermöglicht damit eine selektive Ansteuerung von Tumor- und Knochenmarkszellen.
Das Konzept: Zunächst identifiziert PentixaFor per PET-Bildgebung die CXCR4-Expression und damit geeignete Patienten. Anschließend soll [90Y]Y-PentixaTher gezielt radioaktive Strahlung an die betroffenen Zellen bringen – mit dem Ziel, Tumorlast zu reduzieren und das Knochenmark für die Transplantation vorzubereiten, ohne unnötige Schäden im übrigen Gewebe zu verursachen. Allein in Europa und den USA werden jährlich mehr als 25.000 Stammzelltransplantationen bei AML und MM durchgeführt, jeweils nach vorgelagerter Konditionierung.
Vorgelagerte Radio- statt Chemotherapie
„Die US-amerikanischen IND-Zulassungen stellen eine wichtige regulatorische Validierung unseres CXCR4-gerichteten Ansatzes dar und unterstützen dessen Weiterentwicklung im Setting der Stammzelltransplantation – mit der Kombination aus PentixaFor-Bildgebung und [90Y]Y-PentixaTher“, sagte Dirk Pleimes, CEO der Pentixapharm AG. „AML und MM sind schwerwiegende hämatologische Erkrankungen, bei denen die Transplantation weiterhin ein zentraler Bestandteil der Therapie ist. Wir sind überzeugt, dass eine gezielte Knochenmarkskonditionierung das Potenzial hat, das etablierte chemotherapiebasierte Behandlungsparadigma um einen neuen, differenzierten Ansatz zu erweitern. Diese Entwicklung knüpft an unsere laufenden, von Investigatoren initiierten klinischen Studien in AML in Europa an.“
Kostenintensive Entwicklung steht am Anfang
Der Schritt reiht sich in einen Trend ein: Radiopharmazeutika erleben international einen Aufschwung. Nach Erfolgen in der Prostata- und Neuroendokrin-Tumor-Therapie rücken nun weitere Zielstrukturen und Indikationen in den Fokus. Das Feld ist kapitalintensiv, regulatorisch anspruchsvoll und erfordert spezialisierte Produktions- und Logistikketten für kurzlebige Isotope. Da hat Pentixapharm durch die enge Beziehung zum Isotopenlieferanten Eckert & Ziegler gute Voraussetzungen. Gleichzeitig bietet dieser Bereich die Aussicht, Präzisionsmedizin im wörtlichen Sinne umzusetzen, Diagnostik und Therapie auf denselben molekularen Zielpunkt auszurichten. Pentixapharm ist dabei mit verschiedenen Zielmolekülen und Isotopen unterwegs.
Mit der FDA-Freigabe betritt Pentixapharm nun die nächste klinische Phase in den USA, wo auch eine Studie beim Nierenkarzinom (Diagnostik) schrittweise vorankommt, die bei Erfolg mit einem therapeutischen Pendant ergänzt werden soll. Ob und wann die neue Studie startet, hängt von der weiteren klinischen Strategie und Ressourcenplanung ab. Die Hämatoonkologie wird zunehmend zu einem weiteren Prüfstein für das Potenzial theranostischer Radiopharma-Ansätze.

 Molecular Partners AG
Molecular Partners AG Pentixapharm Holding AG
Pentixapharm Holding AG peterschreibermedia@stock.adobe
peterschreibermedia@stock.adobe