Bayer erhält weitere FDA-Unterstützung für Sevabertinib
Nach der Schnellzulassung des Krebswirkstoffes Sevabertinib im November für vorbehandelte Patienten, haben die FDA und die chinesische CDE Bayers gemeinsam mit dem Broad-Institute (Boston, USA) entwickeltem Molekül den Breakthrough-Status als Erstlinientherapie bei lokal fortgeschrittenem oder metastasiertem HER2-mutiertem NSCLC erteilt.

 Messe München
Messe München
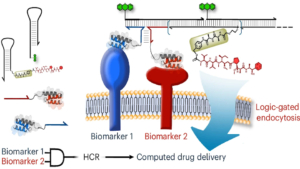 Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0
Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0