
Aufbruch in der klinischen Forschung?
Seit Dezember 2023 gibt es eine Pharmastrategie der Bundesregierung. Damit sollte Deutschland als Forschungs- und Produktionsstandort für die Pharmabranche wieder attraktiver werden. Von der neuen Regierung erhofft man sich eine Fortsetzung.
Die Rahmenbedingungen sollen für die Herstellung und Entwicklung „von Arzneimitteln verbessert, die Digitalisierung im Gesundheitswesen vorangetrieben, Anreize für die Ansiedlung von Produktionsstätten in Deutschland gesetzt und Innovationsprojekte der Pharmaindustrie gefördert“ werden. So stand es im gemeinsamen Papier des Bundesgesundheits-, des Bundeswirtschafts- und des Bundesforschungsministeriums im Dezember 2023. Hat dieses auch heute noch Gültigkeit, oder ist es mit dem Regierungswechsel von der Ampelkoalition auf die jetzige Unions-SPD-Regierung in einer Schublade verschwunden?
Noch hat sich die neue Regierung nicht explizit zur Thematik geäußert. Doch unter Fortführung der durch die damalige Strategie angestoßenen Gesetzesänderungen steht Deutschland bei der klinischen Forschung an einem Wendepunkt. Nach Jahren der Stagnation soll weiterhin die Zahl der Studien wieder gesteigert werden – nicht nur, um den Forschungsstandort zu stärken, sondern auch, um internationale Wettbewerbsfähigkeit zu sichern. Die politischen Rahmenbedingungen wurden zuletzt mit neuen Initiativen wie dem Medizinforschungsgesetz (MFG) und Plattformen wie der ISD (Initiative Studienstandort Deutschland) neu justiert. Doch die Umsetzung bleibt herausfordernd – strukturell, regulatorisch und kulturell.
Aufbruchstimmung ist da
„Wir sind auf einem guten Weg, aber man spürt auch die Ungeduld nach vielen Jahren des Stillstands“, sagt Martin Krauss, Vorsitzender des Bundesverbandes der Medizinischen Auftragsinstitute (BVMA). Die aktuellen politischen Bemühungen, etwa durch das MFG, werden in der Branche durchaus positiv gesehen. So zeigt das Beispiel des 5%-Quorums, dass gezielte Anreize wirken können: Wenn in einer klinischen Studie mindestens 5% der Teilnehmer in Deutschland rekrutiert werden, wird ein innovatives Arzneimittel bei der Erstattung stärker berücksichtigt. „Das hat dazu geführt, dass Pharmafirmen ihre Studienpipeline durchforstet haben – große CROs schließen nun wieder mehr deutsche Zentren ein“, heißt es aus dem BVMA dazu. Auch international zeige sich damit eine Signalwirkung, da Deutschland großen Einfluss auf die Preisbildung in anderen Ländern habe.
USA, China, Europa
Doch der globale Wettbewerb schläft nicht – im Gegenteil. Die Entwicklungen in den USA, etwa bei der Zulassung von Zell- und Gentherapien, werden aufmerksam beobachtet. „Die FDA hat viele Fast-Track-Verfahren ermöglicht, ohne dabei Innovationen zu behindern“, sagt Krauss mit Blick auf aktuelle Änderungen der Verfahrensvoraussetzungen in den USA. Gleichzeitig drohe durch politische Einflussnahme und Populismus ein Rückschritt: „Komplette Expertengremien werden entlassen, Impfstoffe diskreditiert – das wirkt sich negativ auf den globalen Innovationsstandort aus.“ Denn alles hänge doch von den USA ab: Geschäftsmodelle, die Produktstrategie, die Innovationsstrategie. Wenn sich die USA politisch aus bestimmten Bereichen herausnehmen, schicke dies Schockwellen über den Globus, so Branchenexperten im Gespräch mit |transkript. China wiederum setzt langfristig auf Planbarkeit. „Vor zehn Jahren haben sie beschlossen, in den Life Sciences Weltmacht zu werden – heute stehen sie kurz davor“, so einer der häufig gehörten Kommentare auf Branchenevents.
Mit gezielter Öffnung für internationales Kapital werde nun das nächste Kapitel vorbereitet, etwa mit der „NewCo“: ein Joint Venture, das sich teils im Besitz eines chinesischen Unternehmens und teils im Besitz von ausländischen Investoren befindet. Europa hingegen ringe noch mit sich. „Der Wunsch, Europa als stabilen Gegenpol zur US-Dominanz zu positionieren, ist da, aber die Realität sieht anders aus. 60% der weltweiten Pharmaumsätze werden in den USA gemacht, bei nur 4% der Weltbevölkerung. Europa ist fragmentiert, agiert nicht als Einheit“, kommentiert Krauss. Insbesondere der Zugang zu privatem Kapital sei in Europa noch stark eingeschränkt: „Versicherungen investieren bislang nur mit homöopathischen Beträgen. Italien hat dazu kürzlich ein Gesetz verabschiedet: Wenn 10% der Versicherungsmilliarden in Innovation investiert werden, werden die kompletten Kapitalertragssteuern erlassen.“
Hürden in Deutschland
Deutschland selbst kämpft mit altbekannten Problemen: Datenschutz, föderale Strukturen, überbordende Regulierung. „Das Datenschutzthema ist einer der größten Bremsklötze“, heißt es dazu klar aus dem BVMA. Die Auslegung der DSGVO sei hierzulande „weltfremd“ – 17 Landesbeauftragte und ein Bundesbeauftragter für Datenschutz blockierten oft gemeinsam, statt konstruktiv der Innovation den Weg zu bahnen. Das sei forschungsfeindlich vom Prinzip her. Auch bei Ethikkommissionen zeige sich ein zwiespältiges Bild. Das Ziel einer einheitlichen, effizienten Begutachtung ist noch nicht erreicht, auch wenn es Fortschritte bei der Spezialisierung und weiteren Maßnahmen wie Richtlinienkompetenz gebe. Doch eine Konsolidierung fand bisher nicht statt. Und während der Einstieg in die Translation oft noch gelingt, scheitert es häufig am nächsten Schritt: „Der Anfang ist finanziert, aber der Übergang in die großflächige Anwendung – das Valley of Death – ist für viele Firmen kaum zu überwinden“, stellt Ralf Freese, stellvertretender Vorstandsvorsitzender beim BVMA, nüchtern fest. Der Kapitalmarkt sei hier zu wenig begeisterungsfähig, „es fehlt bisher noch der Glaube an den Erfolg“, den man als Innovationsstandort aber benötige.
Die Patienten – kaum im Zentrum
Auch wenn in vielen Papieren vom „Patienten im Mittelpunkt“ die Rede ist, in der Praxis wird das noch unzureichend umgesetzt. „Ärzte sind Versorger, keine Vermittler für die klinische Forschung – die Information über eine mögliche Studienteilnahme erreicht die Patienten kaum“, beklagt Vorstandsmitglied Dr. Yvonne Rollinger. Dabei sei die Bereitschaft vieler Menschen, an klinischen Studien teilzunehmen, generell hoch, wie eine Untersuchung des vfa von 2024 belegt – ein klarer Hinweis darauf, dass hier Potential brachliege.
Dynamik nutzen
Um die lange geforderten gesetzlichen Reformen nun auch in eine breitere Anwendung übersetzen zu können, benötigt die klinische Forschung ein besseres öffentliches Bild: „Deutschland hat exzellente Forschung und sehr hohe Qualität – das müsste viel selbstbewusster kommuniziert werden“, so Krauss. Und selbst die höhere Gründlichkeit könne gut verargumentiert werden: „Langsam ist präzise, präzise ist schnell“, heißt es nicht nur beim Reifenwechsel am Boxenstopp der Formel Eins. Das Plädoyer für die besonnene, aber konsequente Weiterentwicklung der Strukturen verknüpft der BVMA mit dem Appell an die Fortführung der guten Zusammenarbeit aller Beteiligten. Diese habe zu mehr Verständnis für die unterschiedlichen Perspektiven geführt und eine vertrauensvolle Basis geschaffen.
SYMPOSIUM: UMBRUCH UND AUFBRUCH
Beim 33. Symposium der Auftragsforschung in der Klinischen Forschung geht es am 21. November in München um das Leitthema: „Umbruch und Aufbruch – Klinische Forschung wettbewerbsfähig und innovativ gestalten“. Dazu treffen wie gewohnt Experten aus CROs auf Vertreter der Pharma- und Biotechnologieunternehmen, auf Spitzenreferenten aus den Regulierungsbehörden und der Politik sowie auf international versierte Branchenkenner mit Einblicken in die neuesten Änderungen bei der FDA und anderen globalen Strömungen der Verfahrensregeln. Ein Schwerpunkt ist die Patientendatennutzung in der zukünftigen Arzneimittelentwicklung.
Das 33. BVMA-Symposium findet am 21. November 2025 im Holiday Inn Munich – City Centre statt (www.bvma.de)
entnommen aus |transkript 3-2025, Seite 84f

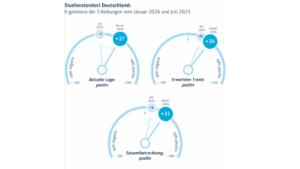 BVMA, vfa, BPI
BVMA, vfa, BPI Rentschler Biopharma SE
Rentschler Biopharma SE BVMA e.V.
BVMA e.V.