Die DNA-Wirkstoff-Konjugate kommen
Mit einer neuen Baukastenmethode aus Genf eröffnen Forscher Möglichkeiten zur über bestimmte Zelloberflächenmarker zielgerichteten zellulären Adressierung von Wirkstoffen, ohne dabei einen Antikörper zu benötigen. Über eine Hybridization Chain Reaction (HCR) genannte Methode wird das Effektormolekül nur wirksam zusammengesetzt, wenn die ausgewählten unterschiedlichen Biomarker auch wirklich gemeinsam auf einer Zelle vorhanden sind.
Die gezielte Verabreichung hochwirksamer Medikamente gehört zu den zentralen Herausforderungen der modernen Onkologie. Einen etablierten Ansatz stellen Antikörper-Wirkstoff-Konjugate (ADCs) dar, bei denen monoklonale Antikörper zytotoxische Substanzen gezielt zu Tumorzellen transportieren. Neue Forschungsergebnisse zeigen nun jedoch einen alternativen Ansatz: DNA-basierte Wirkstoffkonjugate, die mithilfe programmierbarer molekularer Prozesse eine präzisere und potenziell effizientere Medikamentenabgabe ermöglichen. Das beschreiben Nicolas Winssinger und Team vom Department für Organische Chemie der Universität Genf aktuell in Nature Biotechnology.
Grundprinzip: Programmierbare DNA statt statischer Antikörper
Während klassische ADCs aus drei Komponenten bestehen – Antikörper, Wirkstoff/Toxin und Linker –, basiert der neue Ansatz auf sogenannten DNA–Drug Conjugates (DDCs). Hier werden Wirkstoffe an kurze DNA-Strukturen gekoppelt, die sich unter bestimmten Bedingungen selbst zu größeren Komplexen zusammenlagern.
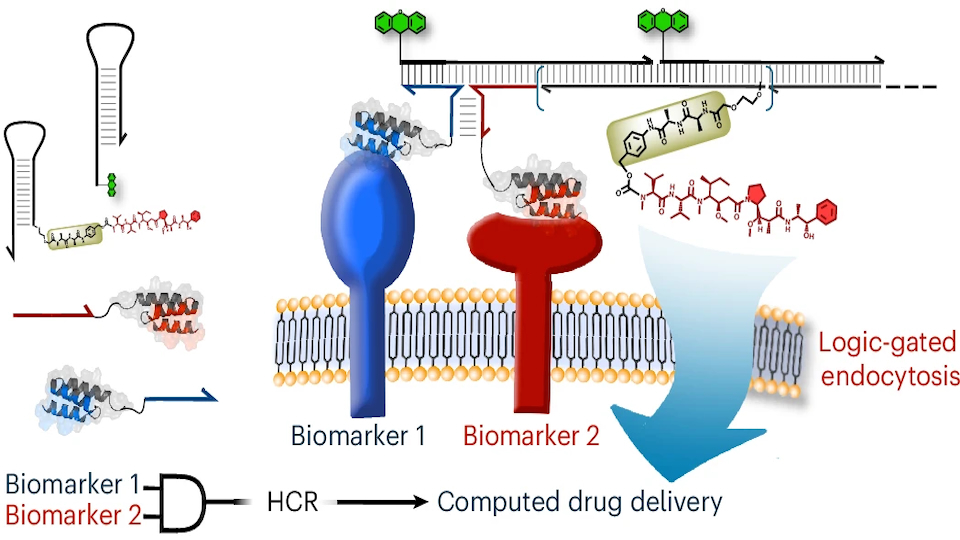
Der entscheidende Unterschied: DNA ist programmierbar. Über definierte Sequenzen lassen sich logische Funktionen („UND“-Verknüpfungen) implementieren, die bestimmen, wann und wo ein Wirkstoff freigesetzt wird. Damit wird die Zielgenauigkeit der Therapie nicht nur über ein einzelnes Oberflächenmerkmal gesteuert, sondern über die Kombination mehrerer Biomarker.
Logikgesteuerte Aktivierung durch Biomarker
Im Zentrum der Methode steht eine sogenannte Hybridization Chain Reaction (HCR). Dabei handelt es sich um eine selbstverstärkende Kettenreaktion von DNA-Strukturen, die erst durch ein spezifisches Signal ausgelöst wird. Dieses Signal entsteht nur, wenn zwei definierte Biomarker gleichzeitig auf der Zelloberfläche vorhanden sind. Spezifische Bindemoleküle (etwa kleine Proteine oder Aptamere) erkennen diese Marker und bringen DNA-Fragmente in räumliche Nähe. Erst dann wird ein „Startsignal“ gebildet, das die Kettenreaktion auslöst.
Das Ergebnis ist eine lokale, stark verstärkte Anreicherung von DNA-Strukturen direkt an der Zielzelle – und damit auch eine gezielte Anreicherung des daran gekoppelten Wirkstoffs. Die Autoren berichten von einer mehr als 100-fachen Verstärkung einer gemessenen Fluoreszenzintensität gegenüber dem ursprünglichen Biomarkersignal.
Verstärkung und flexible Wirkstoffbeladung
Ein wesentlicher Vorteil gegenüber Antikörpern liegt in der Skalierbarkeit: Während ADCs typischerweise nur wenige Wirkstoffmoleküle/Payloads pro Antikörper tragen (meist 2–4), können DNA-basierte Systeme deutlich höhere Wirkstoffmengen akkumulieren. Durch die HCR entstehen polymerartige Strukturen, die zahlreiche auch unterschiedliche Wirkstoffeinheiten aufnehmen können. Dies eröffnet neue Möglichkeiten für kombinatorische Therapien, etwa zur Überwindung von Resistenzen.
Nach der Assemblierung auf der Zelloberfläche werden die DNA-Wirkstoff-Komplexe in die Zelle aufgenommen (Endozytose). Dort werden die Wirkstoffe über enzymatisch spaltbare Linker freigesetzt – ein Prinzip, das auch von ADCs bekannt ist.
Interessanterweise beeinflusst nicht nur die Menge, sondern auch die physikochemische Eigenschaft der Wirkstoffe die Effizienz der Aufnahme. Bestimmte Konfigurationen fördern die Aggregation an der Zellmembran und verstärken so die Internalisierung.
Vergleich zu Antikörper-Wirkstoff-Konjugaten
Im direkten Vergleich zeigen sich grundlegende Unterschiede:
- Zielerkennung:
ADCs basieren meist auf einem einzelnen Biomarker. DDCs können mehrere Marker logisch verknüpfen und so die Selektivität erhöhen. - Molekülgröße und Penetration:
Antikörper sind große Proteine (~150 kDa), deren Eindringen in Tumorgewebe begrenzt ist. Kleinere DNA-basierte Systeme könnten hier Vorteile bieten (was noch zu beweisen ist). - Wirkstoffbeladung:
ADCs sind in ihrer Beladung limitiert, während DNA-Systeme durch Selbstassemblierung hohe Wirkstoffdichten erreichen können. - Flexibilität und Modularität:
DNA erlaubt eine programmierbare Kombination von Zielstrukturen und Wirkstoffen – ein Ansatz, der stärker in Richtung personalisierte Medizin weist.
Potenzial und Herausforderungen
Die Technologie eröffnet die Möglichkeit, Therapien nicht nur zielgerichteter, sondern auch „intelligenter“ zu gestalten – indem sie nur unter exakt definierten biologischen Bedingungen aktiv wird. Gleichzeitig bestehen noch Herausforderungen, etwa hinsichtlich der Stabilität von DNA im Körper oder der klinischen Übertragbarkeit.
Dennoch zeigt der Ansatz, wie sich Prinzipien der DNA-Nanotechnologie mit der Wirkstoffentwicklung verbinden lassen. Im Vergleich zu klassischen Antikörper-basierten Strategien könnte dies einen Paradigmenwechsel hin zu stärker programmierbaren und modularen Therapiesystemen einleiten. Auch in der Herstellung und Herstellbarkeit dürfte eine auf Nukleinsäuremodule gerichtete Therapieentität von der Kosteneffizienz und Skalierbarkeit den Antikörpern deutlich überlegen sein. Doch vor der eventuellen Marktdurchdringung liegen noch viele Jahre und weitere Schritte in der Validierung und Prozessoptimierung.


 Novartis
Novartis beermedia - stock.adobe.com
beermedia - stock.adobe.com