
Schweizer Datenbank für Medizinprodukte online
Seit einigen Tag ist das erste von zwei Modulen der neuen Medizinproduktedatenbank swissdamed online. Darin können Hersteller sich sowie ihre Medizinprodukte und In-vitro-Diagnostika für den Schweizer Markt registrieren. Die Datenbank soll einen Überblick über die Schweizer Medizintechnikbranche und ihre Produkte geben.
Die schrittweise Einführung der neuen Medizinprodukte-Plattform der Schweizerischen Zulassungs- und Aufsichtsbehörde für Arzneimittel und Medizinprodukte Swissmedic hat Anfang August begonnen. Die Plattform swissdamed gleicht in ihrem Aufbau der europäischen Datenbank EUDAMED. Damit soll die Gleichwertigkeit zwischen den Regulierungen der Schweiz und der EU möglichst erhalten bleiben und der Aufwand für Wirtschaftsakteure minimiert werden.
Überblick über Schweizer Markt
Ziel der neuen Plattform ist es, einen Überblick über die Medizintechnik-Hersteller, ihre Produkte sowie In-vitro-Diagnostika auf dem Schweizer Markt zu geben und so mehr Transparenz zu erhalten. Dafür werden Informationen über die Medizinprodukte und die an ihnen beteiligten Unternehmen gesammelt, bearbeitet und publiziert.
Zwei Module
Die Datenbank umfasst zwei Module (Actors-Modul und Devices-Modul) und eine frei zugängliche Webseite. Dort werden ab sofort die Wirtschaftsakteure und im Verlaufe des Jahres 2025 auch (freiwillig) bestimmte Medizinprodukte registriert.
Als erstes Modul wurde Actors freigeschaltet. Das zweite, sogenannte Devices-Modul, soll in mehreren Etappen aufgeschaltet werden: nach dem ersten Release im kommenden Jahr können bestimmte Produkte registriert werden. Dabei handelt es sich um Regulation Devices (MDR und IVDR), welche mittels XML-Datei im EUDAMED-Format hochgeladen werden. Weitere Releases werden schließlich das Devices-Modul vervollständigen.
Erst mit einem ausreichenden Ausbau der swissdamed und entsprechenden Änderung der Medizinprodukteverordnun und der Verordnung über In-vitro-Diagnostika wird die Produktregistrierung verpflichtend.
Zu swissdamed

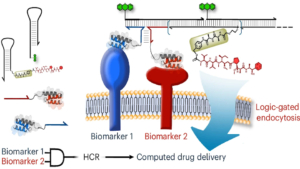 Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0
Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0 Novartis
Novartis beermedia - stock.adobe.com
beermedia - stock.adobe.com