
4SC: statt Freude Tränen der Trauer
Zum Jahreswechsel zeigte sich die Martinsrieder 4SC AG noch zuversichtlich: auf den letzten Metern des Zulasungsprozesses für das Krebsmittel Resminostat hatte die europäische Zulassungsbehörde EMA zwar Rückfragen gestellt, doch diese waren nach Ansicht von 4SC vollumfänglich beantwortet worden. Nun folgt eine erneute Rückmeldung der EMA, die besagt, der Antrag sei nicht genehmigungsfähig, es bestünden „schwerwiegende Einwände“. Der Aktienkurs rauscht in den Keller.
Man würde so gern genauer auf den Briefwechsel zwischen der EMA und der Martinsrieder 4SC AG (Frankfurter Wertpapierbörse, Prime Standard: VSC) schauen. Welche Fragen wurden dem bereits 1997 gegründeten Biotech-Unternehmen zum Jahresende vom Ausschuss für Humanarzneimittel (CHMP) gestellt? Und wie lauteten die Antworten, die das über die Jahre immer kleiner gewordene Team um CEO Jason Loveridge zurück nach Amsterdam schickte, um Anfang Januar mitzuteilen, dass man diese vollumfänglich beantwortet habe?
Nun informiert der 4SC- Vorstand über die Entscheidung der Europäischen Arzneimittelagentur (EMA), dass der Antrag für Resminostat (Kinselby) „nach Prüfung der endgültigen Daten und der Antworten des Unternehmens auf Fragen derzeit nicht genehmigungsfähig ist“. Es seien „schwerwiegende Einwände“, sogenannte Major Objections, festgestellt worden, die die Empfehlung für die Marktzulassung zum jetzigen Zeitpunkt ausschlössen.
Die 4SC AG werde nun das EMA-Feedback auswerten und entscheiden, wie am besten auf die Einwände und die Liste der offenen Fragen innerhalb der Frist von einem Monat reagiert. Das sind die Äußerungen eines leicht ratlos wirkenden Managements, das wohl selbst überrascht ist von dieser ungünstigen Wendung. Ob noch etwas zu retten ist? Die Börsianer haben reagiert und den Daumen deutlich gesenkt. Wenn man die Fragen von damals, die damaligen Antworten und die neuerlichen Fragen und Bedenken der EMA nicht wirklich kennt, bleibt es reine Spekulation, ob noch ein Fünkchen Hoffnung ist oder aus dieser Situation kaum ein Ausweg möglich sein wird.
Die zulassungsrelevante RESMAIN-Studie hatte gezeigt, dass Resminostat (Kinselby) als Erhaltungstherapie bei fortgeschrittenem CTCL das Fortschreiten der Krankheit signifikant verzögert. Patienten hatten ein längeres progressionsfreies Überleben (8,3 vs. 4,2 Monate bei Placebo) und eine verdoppelte Zeit bis zur nächsten Behandlung. Nebenwirkungen waren meist mild. Der EU-Zulassungsantrag war Anfang 2024 eingereicht worden. Welcher Teil der Datenpakete nun so kritische Rückfragen oder sogar das Aus des Zulassungsverfahrens bewirkt hat, bleibt bisher im Dunkeln. 4SC ist ein Portfoliounternehmen mit rund 70% Aktienbesitz in Beteiligungsgesellschaften der Gebrüder Strüngmann. Ob die Milliardäre ein Weitermachen finanzieren werden, nachdem sie gerade Ende des vergangenen Jahres noch einmal rund 4 Mio. Euro zugeschossen haben, bleibt ebenfalls abzuwarten.

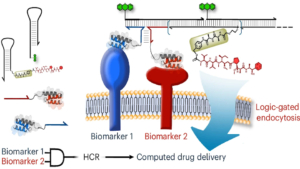 Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0
Chen SK et al, Nature Biotechnology (2026). https://doi.org/10.1038/s41587-026-03044-0 peterschreiber.media – stock.adobe.com
peterschreiber.media – stock.adobe.com InnovationLab GmbH | Luks Adler
InnovationLab GmbH | Luks Adler