MASH-Therapeutika – die neuen Blockbuster-Medikamente?
Ein Hintergrund zu neuen Wirkstoffen und der Konkurrenzsituation in der Entwicklung bei der Indikation Leberfibrose.
von Dr. Michael Thiel
MASH (früher NASH) steht für Metabolische Dysfunktions-assoziierte Steatohepatitis. Sie ist die am häufigsten vorkommende Form der Leberfibrose. Als Leberfibrose wird der Umbau von gesundem Lebergewebe in Narbengewebe infolge chronischer Entzündungen beschrieben. Diese können durch eine Fettleber, übermäßigen Alkoholgenuss oder chronische Virushepatitis (B, C) entstehen. Die Leberfibrose wird nach dem Desmet-Schema in vier Stadien unterteilt, das Endstadium F4 ist die Leberzirrhose. Die globale Prävalenz der fortgeschrittenen Leberfibrose im Stadium F2/F3 wird mit 3,5 bis 4% angegeben, die globale Prävalenz der Leberzirrhose mit 1,2%. Jährlich sterben etwa 1,2 Millionen Menschen an einer Leberzirrhose. Die Zahl der Patienten mit einer Fettleber stieg in den vergangenen Jahren sprunghaft an, parallel zur hohen Zahl der Patienten mit Adipositas und Diabetes Mellitus. Bis zum Jahr 2024 gab es keine Möglichkeit der medikamentösen Behandlung von Patienten mit Leberfibrose. Man konnte entweder die Grunderkrankungen behandeln oder der Patient hatte Glück und es wurde eine Spenderleber gefunden. Ansonsten war der Krankheitsverlauf tödlich.
Rezdiffra – das erste MASH-Therapeutikum
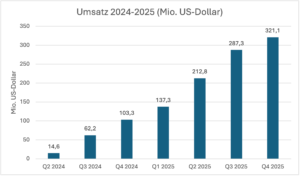
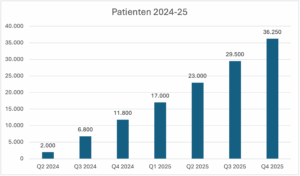
Am 14. März 2024 erhielt das amerikanische Biotech-Unternehmen Madrigal Pharmaceuticals von der FDA die weltweit erste Zulassung zur medikamentösen Behandlung von MASH-Patienten im Stadium F2/F3. Der Wirkstoff ist Resmetirom (Handelsname: Rezdiffra), ein THR-Beta-Agonist, der täglich oral in der Dosierung 80 mg/100 mg verabereicht wird. Die Therapie ist gut verträglich, nach einjähriger Gabe konnte eine Verbesserung der Leberfibrose bis zu einer Stufe festgestellt werden. Die jährlichen Therapiekosten belaufen sich auf 51.000 USD. Wie Abb. 1a und 1b zu entnehmen ist, entwickelt sich Rezdiffra in den USA zu einem Blockbuster-Medikament. Der Umsatz erreichte im vierten Quartal 2025 321 Mio. USD. Mittlerweile werden über 36.000 Patienten mit dem Medikament behandelt.
Der Madrigal-Aktienkurs stieg im Jahr 2025 von 311 USD auf 506 USD. Am 19. April 2025 erhielt Rezdiffra die conditional marketing authorization von der Europäischen Kommission, im September 2025 wurde das Medikament in Deutschland eingeführt. Momentan läuft eine Phase III-Studie mit Leberzirrhose-Patienten im Stadium F4c zur Erweiterung der Indikation. Zur optimalen Ausschöpfung des Patientenpotentials für den Marktführer Rezdiffra arbeitet man bei Madrigal Pharmaceuticals zielstrebig an einer Kombinationsstrategie. Die erste Fixkombination wird mit einem GLP1-Rezeptor-Agonisten angestrebt. Zu diesem Zweck wurde im Juli 2025 der Wirkstoff SYH2086 von der chinesischen Firma CSPC Pharmaceuticals für ein Down Payment von 120 Mio. USD einlizenziert. Ziel ist die Entwicklung einer one-pill für Diabetes-Patienten mit Fettleber – ein global riesiges Patientenpotential. Das zweite Fixkombinationsprojekt ist seit Januar 2026 bekannt: Für 50 Mio. USD wurde der DGAT-2-Inhibitor Ervogastat von Pfizer einlizenziert. Ervogastat ist in der Phase II und zeigte gute Ergebnisse bei der Reduktion des Leberfetts. Das dritte Projekt ist die Kombination von Rezdiffra mit siRNAs. Im Februar 2026 wurden sechs präklinische siRNA-Programme von der chinesischen Firma Suzhou Ribo Life Sciences für 60 Mio. USD Upfront und bis zu 4,4 Mrd. USD an Meilensteinzahlungen einlizenziert.
Bei Madrigal Pharma hat man das riesige Marktpotential zur Therapie der Leberfibrose erkannt und möchte die First Mover Situation konsequent ausnutzen und ein Produktportfolio aufbauen, dass alle MASH-Patienten bedienen kann. Die MASH-Pipeline von Madrigal Pharmaceuticals umfasst Stand Februar 2026 zehn Programme.
Die Konkurrenz (siehe Abb.2)
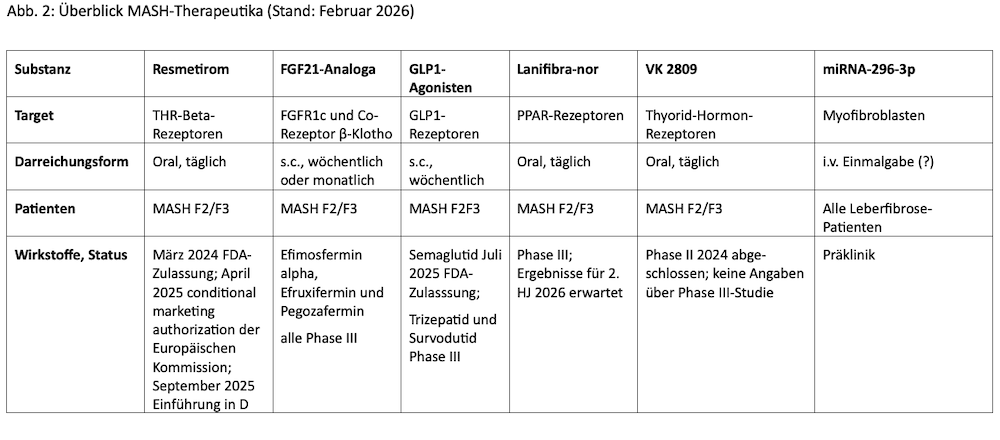
- FGF21-Analoga
Hauptkonkurrenten für Rezdiffra dürften die FGF21-Analoga sein. Der Fibroblasten-Wachstumsfaktor 21 (FGF21) ist ein potenter endokriner Regulator mit physiologischen Auswirkungen auf den Glukose- und Lipidstoffwechsel. Er signalisiert über einen heteromeren Rezeptorkomplex, der aus dem FGF-Rezeptor 1c (FGFR1c) und dem Co-Rezeptor beta-Klotho besteht. In der Leber fördert FGF21 die Fettsäureoxidation und verringert die Lipogenese, wodurch sich das Leberfett reduziert und der systemische Triglyceridspiegel sinkt. Drei FGF21-Analoga befinden sich momentan in der klinischen Phase III zur Behandlung von MASH-Patienten im Stadium F2/F3: Efimosfermin alpha, Efruxifermin und Pegozafermin. In den vorliegenden klinischen Studien kam es zu einer signifikanten Verbesserung der Leberfibrose bei guter Verträglichkeit. Die Medikamente werden s.c. verabreicht, entweder einmal wöchentlich oder einmal monatlich. Wohl bedingt durch den Markterfolg von Rezdiffra kam es im Jahr 2025 zu bemerkenswert teuren Akquisitionen der drei oben genannten FGF21-Analoga: GSK übernahm im Mai 2025 Boston Pharmaceuticals (Wirkstoff: Efimosfermin alpha) für 1,2 Mrd. USD Upfront und 800 Mio. USD Milestone Payments. Im September kaufte Roche 89bio (Wirkstoff: Pegozafermin) für 3,5 Mrd. USD. Zu guter Letzt hat Novo Nordisk im Oktober letzten Jahres Akero Therapeutics (Wirkstoff: Efruxifermin) für 4,7 Mrd. USD übernommen.
- GLP-1-Agonisten
Ebenfalls in der klinischen Phase III zur Behandlung von MASH-Patienten im Stadium F2/F3 befinden sich die GLP-1-Agonisten Trizepatid (E. Lilly) und Survodutid (Boehringer Ingelheim). Semaglutid (NovoNordisk) erhielt im Juli 2025 die FDA-Zulassung für die Behandlung von MASH-Patienten im Stadium F2/F3, entschied sich aber trotzdem für die Akquisition des FGF21-Analogons Efruxifermin. Über den Grund kann nur spekuliert werden. Vielleicht möchte man bei Novo Nordisk nicht das Diabetes- und Abnehmgeschäft mit Semaglutid kannibalisieren? Die GLP-1-Agonisten müssen einmal wöchentlich s.c. appliziert werden.
- Lanifibranor
Der PPA-Agonist Lanifibranor von Inventiva Pharma befindet sich ebenfalls in der klinischen Phase III-Studie zur Behandlung von MASH-Patienten im Stadium F2/F3, der Wirkstoff wird täglich oral verabreicht. Studienergebnisse werden im zweiten Halbjahr 2026 erwartet.
- VK 2809
Der Thyroid Hormone Receptor Agonist VK 2809 von Viking Pharma, hat im zweiten Quartal 2024 die Phase II-Studie abgeschlossen, in der die signifikante Reduktion von Leberfett nachgewiesen werden konnte. Über eine klinische Phase III-Studie mit VK 2809 gibt es keine Informationen.
- miRNA-296-3p
Der gentechnische Ansatz mit miRNA-296-3p ist ein Projekt der Professoren Michael Ott und Amar Deep Sharma an der Medizinischen Hochschule Hannover. Es ist der erste medikamentöse Leberfibrose-Ansatz, der direkt an den hepatischen Myofibroblasten ansetzt, wo sich die Fibrose entwickelt. In ersten präklinischen Studien mit Mäusen und menschlichen Leberzellen konnte gezeigt werden, dass sich die Fibrose bei der Gabe von miRNA-296-3p signifikant zurückentwickelt (siehe auch J. Markovic et.al.: Identification and functional validation of miR-190b-5p and miR-296-3p as novel therapeutic attenuators of liver fibrosis. Journal of Hepatology 2025, Vol. 82, 301-314). Die beiden Forscher gehen davon aus, dass bei den meisten Patienten eine einmalige intravenöse Gabe von miRNA-296-3p ausreichen wird. Der Therapieerfolg soll anhand der gängigen Biomarker für die Leber verfolgt werden, gegebenenfalls ist eine Wiederholungsbehandlung notwendig. Ein großer Vorteil der Behandlung mit miRNA-296-3p wäre, dass das Medikament bei allen Formen der Leberfibrose, sei es metabolisch, Alkohol- oder viral bedingt, eingesetzt werden könnte.
Ausblick
Mit Resmetirom und den weiteren Wirkstoffen in Phase III eröffnet sich erstmals die Möglichkeit der effektiven Behandlung von MASH-Patienten im Stadium F2/F3. Das Potential der bis dato unbehandelten Patienten ist sehr groß, die Zahl der Patienten mit Adipositas und/oder Diabetes Mellitus in den letzten Jahren sprunghaft gestiegen. Rezdiffra hat nach knapp anderthalb Jahren der Vermarktung – nur auf dem amerikanischen Markt – bereits Blockbuster-Status. Die Behandlungskosten pro Patient betragen 51.000 USD pro Jahr, die Preise der Konkurrenzprodukte werden sich wohl in diesem Rahmen bewegen. Mit der zielstrebigen Kombinationsstrategie will Madrigal Pharmaceuticals seine Marktführerposition weiter ausbauen.
Der Vorteil der Konkurrenzpräparate liegt darin, dass sie einmal wöchentlich oder nur einmal monatlich s.c. gegeben werden müssen. Rezdiffra muss täglich oral eingenommen werden. Ein Game-Changer könnte der Wirkstoff miRNA-296-3p werden, der direkt in den hepatischen Myofibroblasten ansetzt. Eine einmalige intravenöse Gabe könnte genügen, alle Patienten mit Leberfibrose, ob mit metabolischem, viralem oder alkoholischem Hintergrund, effektiv zu behandeln. Doch der Wirkstoff miRNA-296-3p befindet sich erst in der präklinischen Entwicklung. Bis ein miRNA-296-3p Arzneimittel auf den Markt kommt, können noch leicht 8 bis 10 Jahre vergehen.
Autor:
Dr. Michael Thiel, Kooperationspartner SANEMUS AG, Mannhardtstr. 6, 80538 München, Kontakt: michael.thiel@sanemus.com

 Daniel Fuhr - stock.adobe.com
Daniel Fuhr - stock.adobe.com Boehringer Ingelheim
Boehringer Ingelheim