Räumliche Proteomik enthüllt lebensrettenden Therapieansatz
Einem internationalen Forschungsteam ist es gelungen, mit Hilfe einer hochmodernen räumlichen Proteomik-Technologie den Signalweg einer bisher unheilbaren und oft tödlich verlaufenden Entzündungsreaktion der Haut aufzuklären und dadurch eine erfolgreiche Therapiemöglichkeit zu identifizieren.
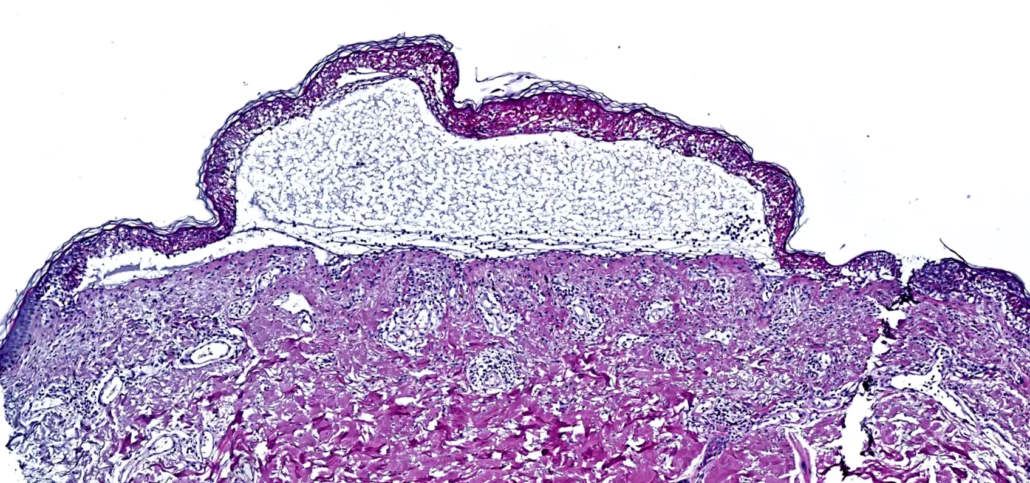
Das ist translationale Medizin par excellence: Das Team um Matthias Mann vom Max-Planck-Institut für Biochemie in Martinsried beschreibt kürzlich in Nature seinen hochmodernen Ansatz für räumliche Proteomik: Deep Visual Proteomics (DVP) – und dessen herausragenden Nutzen in der Therapieentwicklung. Die Forscher untersuchten Hautproben von Patienten mit toxischer epidermaler Nekrolyse (TEN) – bekannt als Stevens-Johnson-Syndrom (SJS) –, einer seltenen, aber lebensbedrohlichen Nebenwirkung einiger Medikamente und Antibiotika, bei der es zur Blasenbildung und Ablösung der Epidermis kommt. Mit Hilfe ihres Proteomik-Ansatzes gelang es, eine Karte von Tausenden Proteinen in einzelnen Zellen zu erstellen, die eine Überaktivierung des entzündungsfördernden JAK/STAT-Signalwegs aufzeigt und somit passende Inhibitoren als mögliche Therapie nahelegt.
Die Deep Visual Proteomics-Technologie wurde erst vor zwei Jahren in Manns Labor entwickelt. Sie verbindet fortschrittliche Mikroskopie, KI-gestützte Analyse und lasergeführte Mikrodissektion mit hochempfindlicher Massenspektrometrie. Untersucht wurden Hautproben von Patienten mit milden und schweren TEN-Ausprägungen sowie von gesunden Personen. Durch spezifische Färbungen in Gewebeschnitten ließen sich Keratinozyten und Lymphozyten identifizieren und mit einem fokussierten Laserstrahl präzise für die anschließende massenspektrometrische Messung isolieren. Auf diese Weise konnte in den Zelltypen das Profil von jeweils rund 5.000 Proteinen analysiert werden. Die Ergebnisse legten eine starke Interferon-abhängige Entzündungsantwort im Bereich der Blasenbildung sowie eine starke Aktivierung des JAK/STAT-Signalwegs nahe.
Bisher gab es für die gravierende Erkrankung TEN keine Therapiemöglichkeit. JAK-Inhibitoren allerdings werden bereits für die Behandlung von Entzündungserkrankungen wie rheumatoider Arthritis eingesetzt. Daher testeten die Forscher verschiedene dieser Medikamente zunächst in vitro und in verschiedenen Mausmodellen und konnten damit sowohl die Entzündungsreaktionen als auch das Absterben von Keratinozyten deutlich verringern. In Zusammenarbeit mit der Ludwig-Maximilians-Universität München und der Fuijan Medical University in Fuzhou, China, wurden dann sieben Patienten außerhalb des zugelassenen Gebrauchs mit einem JAK-Inhibitor behandelt, die allesamt eine schnelle Verbesserung zeigten.
Es sei das erste Mal, dass eine räumliche Omics-Technologie eine unmittelbare und greifbare Auswirkung in der Klinik habe, sagte der Hauptautor Matthias Mann. Er sieht weitere Möglichkeiten für medizinische Durchbrüche: „Dieser Ansatz könnte auf eine Vielzahl von Krankheiten angewendet werden und potentiell die Medikamentenentdeckung in vielen Bereichen der Medizin beschleunigen.“

 Jan Krönke
Jan Krönke