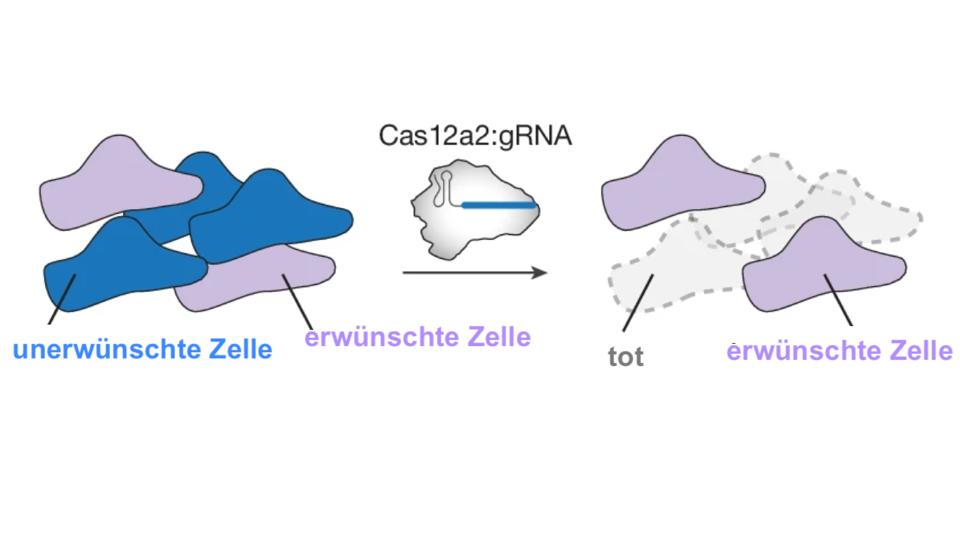
RNA-sequenzspezifische Waffe: CRISPR-Cas12a2 eliminiert gezielt
Ein internationales Forschungsteam unter Beteiligung von Akribion Therapeutics sowie von Forschern aus Würzburg hat ein neues CRISPR-Verfahren entwickelt, mit dem sich einzelne Zellen anhand ihrer RNA-Signatur gezielt eliminieren lassen. Die in Nature veröffentlichte Arbeit zur Nuklease Cas12a2 eröffnet potenzielle Anwendungen in Onkologie, bei Autoimmunerkrankungen sowie in der Infektionsmedizin und verschafft der Gentherapie eine hochspezifische Waffe.
Ein internationales Forschungsteam aus akademischen Einrichtungen und Industriepartnern hat ein neues CRISPR-basiertes Verfahren entwickelt, mit dem sich einzelne Zellen anhand ihrer RNA-Signatur gezielt abtöten lassen. Die jetzt im Fachjournal Nature veröffentlichten Ergebnisse könnten neue Anwendungen in Medizin, Biotechnologie und Landwirtschaft ermöglichen – etwa bei der Entfernung virusinfizierter Zellen, mutierter Tumorzellen oder fehlerhaft editierter Zellpopulationen.
Entdeckt von Brain Biotech im Metagenom
Beteiligt an der Arbeit waren das Helmholtz-Institut für RNA-basierte Infektionsforschung (HIRI), das Helmholtz-Zentrum für Infektionsforschung, die Julius-Maximilians-Universität Würzburg, die University of Utah und die Utah State University sowie Akribion Therapeutics. Akribion ist eine Abspaltung der hessischen Brain Biotech AG, die bei einer gezielten Suche im Metagenom des Mikrobenreiches eine große Zahl CRISPR-ähnlicher Genomeditierungswerkzeuge gefunden hatte. Diese wiesen ganz unterschiedliche extra Spezialitäten zur bekannten CRISPR/Cas9-Einheit auf. Für einige dieser Moleküle hat Akribion Therapeutics in einem exklusiven Technologielizenzvertrag mit Brain Biotech die Rechte für die weitere Nutzung eingeräumt bekommen und entwickelt diese für therapeutische Zwecke und betimmte Krebsindikationen weiter.
Im Mittelpunkt der Studie in Nature steht die CRISPR-Nuklease Cas12a2. Anders als klassische Genomeditierungswerkzeuge wie Cas9, die gezielt einzelne DNA-Sequenzen schneiden, löst Cas12a2 nach Aktivierung durch eine spezifische RNA-Sequenz eine umfassende Zerstörung von Nukleinsäuren in der Zelle aus. Dadurch sterben die betroffenen Zellen ab. „Das führt zu umfangreichen DNA-Schäden in Bakterien, wodurch deren Wachstum gestoppt und somit die Ausbreitung eines erkannten Eindringlings verhindert wird“, sagte Chase Beisel, affiliierter Abteilungsleiter am HIRI und Mitautor der Studie.
Während die Wirkung des Systems in Bakterien bereits bekannt war, blieb bislang offen, wie Cas12a2 in eukaryotischen Zellen reagieren würde. Das Forschungsteam konnte nun zeigen, dass die Nuklease auch in Hefe- und menschlichen Zellen gezielt jene Zellen eliminiert, die das jeweilige Zieltranskript enthalten, während andere Zellen verschont bleiben.
Proof-of-Principle schafft neue Waffe gegen geschädigte Zellen
„Im Gegensatz zu aktiviertem Cas9, das eine einzelne präzise Schnittstelle in der gebundenen DNA erzeugt, zerschneidet RNA-aktiviertes Cas12a2 alle DNA, die es antrifft, und tötet so die Zelle“, erklärte Ryan Jackson von der Universität Utah. „Sein Ziel ist es nicht, irgendetwas zu korrigieren. Stattdessen zerstört es alles, was es sieht“, ergänzte Yang Liu, ebenfalls aus Utah, USA. Nach Angaben der Autoren zeigte die Methode eine hohe Sequenzspezifität und Sensitivität gegenüber Fehlpaarungen, ohne messbare Off-Target-Effekte.
Die Forscher demonstrierten das Potenzial der Technologie unter anderem an virusinfizierten Zellen sowie an Krebszellen mit spezifischen Punktmutationen. Zudem gelang es, nicht erfolgreich editierte Zellen aus Zellpopulationen zu entfernen und damit die Qualität von Genomeditierungen zu verbessern.
„Unsere Technologie bietet uns ein leistungsstarkes Werkzeug zur sequenzspezifischen Abtötung krankheitserregender Zellen“, sagte Paul Scholz von Akribion Therapeutics, Erst- und korrespondierender Autor der Publikation und im Unternehmen Leiter der Forschung und Entwicklung. „In dieser Studie demonstrieren wir das Potenzial unserer Technologie, indem wir virusinfizierte Zellen sowie durch eine punktuelle Mutation veränderte Krebszellen ins Visier nehmen. Unsere Technologie lässt sich jedoch so programmieren, dass sie nahezu jede gewünschte RNA-Signatur adressieren kann.“
Die Autoren sehen mögliche Anwendungen von der Onkologie über chronische Infektionen bis hin zur Landwirtschaft. Besonders relevant könnte der Ansatz für künftige Zell- und Gentherapien werden, da sich Zellen erstmals direkt anhand ihres Transkriptoms selektiv ausschalten lassen.
Genereller Ausschaltknopf gefunden?
„Da Cas12a2 mit einer Leit-RNA so programmiert werden kann, dass es auf jede beliebige RNA-Sequenz abzielt, und da es kaum oder gar keine sogenannten Off-Target-Effekte zeigt, glauben wir, einen Weg gefunden zu haben, um Zellen in allen Bereichen der Biologie selektiv auszuschalten“, sagte Jackson.
Auch die beteiligten Wissenschaftler sehen die aktuelle Arbeit zunächst als Ausgangspunkt für weitere Entwicklungen. „Wir hoffen, dass die Forschungsgemeinschaft diese neuen Möglichkeiten genauer untersuchen wird und herausfindet, wie sie über unsere Proof-of-Principle-Studie hinaus weiter verbessert und angewendet werden können“, erklärte Beisel. Parallel dazu arbeitet das Team von Akribion bereits daran, Cas12a2 für klinische Anwendungen weiterzuentwickeln.
Als Mitautor des Nature-Artikels ist auch Dr. Michael Krohn aufgeführt, Co-Gründer und Co-CEO von Akribion Therapeutics. Er zeigt sich extrem erfreut und stolz auf die Publikation, die nun erstmals die Technologieplattform und ihre „Power“ mit In-vivo-Daten unterlege. „Wir sind erst seit Dezember 2024 als eigenständiges Unternehmen unterwegs. Initial haben wir uns auf HPV-assoziierten Kopf- und Nacken-Tumor konzentriert, doch das ist erst der Anfang. Wir denken schon an weitere Indikationsgebiete wie Autoimmunerkrankungen, Fibrosen und Infektionskrankheiten.“
Man darf gespannt sein, welche Möglichkeiten dieses und auch die anderen spezifischen CRISPR-Werkzeuge aus dem Hause Brain Biotech noch eröffnen. Im Wettstreit mit der kostenträchtigen Zelltherapie könnten diese Formen von Genomeditierung, die weniger auf Reparatur aus sind, als auf die Zerstörung von geschädigten oder infizierten Zellen, eine neue Tür für die sequenzgerichtete Gentherapie öffnen.
Originalpublikation: Paul Scholz et al.; RNA-triggered cell killing with CRISPR–Cas12a2; Nature, Mai 2026, DOI: 10.1038/s41586-026-10466-y

 Biontech SE
Biontech SE Boehringer Ingelheim
Boehringer Ingelheim Proxygen GmbH
Proxygen GmbH