Kaum ein Tag vergeht, an dem nicht einer der einschlägigen Pharma- und Biotechnologieverbände zur Kritik an aktuellen Gesetzgebungsvorhaben oder daraus folgenden neuen Regelungen ansetzt. Jedesmal wird dabei der "Innovationsstandort" Deutschland beschworen und die meisten Änderungen werden als schädlich bezeichnet. Nun gilt die nächste Alarmstufe rot den Biosimilars und der angedachten "automatischen Substitution".
ANZEIGE
Zum ersten Mal hat ein Impfstoff gegen die von Mücken übertragene Viruskrankheit Chikungunya eine Phase III-Studie bestanden. Der vom österreichisch-französischen Biotech-Unternehmen Valneva entwickelte monovalente Lebendimpfstoff VLA1553 führte bei 98,9 Prozent der Studienteilnehmer 28 Tage nach einer einmaligen Impfung zu virusneutralisierenden Antikörperspiegeln, die bis zu 180 Tage nach der Impfung anhielten. Zulassungsanträge für die USA, Kanada und Europa seien bereits eingereicht, teilte Valneva mit.
Der Saatgutspezialist KWS Saat SE & Co. KGaA und das Berliner Start-up-Unternehmen VF Nutrition GmbH, besser bekannt unter dem Markennamen vly, gehen eine mehrjährige Entwicklungspartnerschaft ein. Die beiden Unternehmen arbeiten gemeinsam daran, die Entwicklung von Lebensmitteln auf Basis von Erbsenprotein voranzutreiben.
Mit einem symbolischen Knopfdruck hat die Garchinger ITM Isotope Technologies Munich SE in Neufahrn bei Freising die weltweit größte Produktionsanlage für das Radionuklid Lutetium-177 eröffnet. Bis die Produktion nach Abschluss aller Genehmigungsverfahren tatsächlich hochgefahren werden kann, werden allerdings noch einige Monate vergehen, die Rede ist von Mitte 2024. Die Nachfrage nach Radiopharmazeutika ist so stark gestiegen, dass die bisherigen Produktionsräume in Garching aus allen Nähten platzen und man im Drei-Schicht-Betrieb rund um die Uhr arbeiten muss.
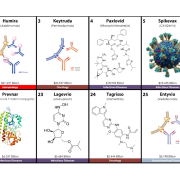
Jon Tryggvi Njardasons TOP-200-Pharma-Liste hat sich zu einem Klassiker der jährlichen Zahlenerhebungen entwickelt und wird in seiner Forschungsgruppe in Tuscon Arizona, USA, jährlich anhand der weltweiten Verkaufszahlen für Pharmazeutika von Studenten erstellt. Für 2022 sind diesmal die beiden ersten Top-Plazierungen mit einem "made in Germany" versehen: Comirnaty und Humira. Zusammen stehen sie für knapp 60 Mrd. US-Dollar Umsatzerlöse.
Die PentixaPharm GmbH, ein Entwickler innovativer Radiopharmazeutika und 100-prozentige Tochter der Eckert & Ziegler Strahlen- und Medizintechnik AG (ISIN DE0005659700; TecDax), hat vom Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) die Genehmigung zum Start der offenen Dosiseskalationsstudie von PentixaTher erhalten. Der mit Yttrium-90 markierte CXCR4-Wirkstoff wird als Strahlentherapeutikum zur Behandlung von rezidivierten oder refraktären primären oder isolierten sekundären Lymphomen des zentralen Nervensystems getestet.
Europäischer Zusammenschluss von Real-World-Data-Spezialisten: die Schweizer BC Platforms (Zürich) übernimmt die skandinavische 4Pharma (Hauptsitz in Turku, Finnland, Niederlassung in Lund, Schweden), die ein eingeführter Anbieter von medizinischen Forschungsdaten und Analysedienstleistungen für globale klinische Studien und Real-World-Daten ist.
Eine knappe Kursverdoppelung der Morphosys-Aktie freut derzeit Aktionäre, die den vorhergehenden langanhaltenden Niedergang nicht mitgemacht haben und bei den niedrigen Börsenständen eingestiegen sind. Richtiggehende Neuigkeiten haben die Martinsrieder nicht vermeldet, und auch die Meinungen der Analysten sind zweigeteilt.
Die Garchinger Radiopharmaziefirma ITM SE kündigt eine Investitionsrunde in Höhe von 255 Mio. Euro an und plant, die radiopharmazeutische Pipeline voranzutreiben und die Produktionskapazitäten für Radioisotope zu erweitern. Mit Athos kommt ein neuer Investor hinzu, hinter dem bekanntlich die Strüngmann Brüder stecken.
Die ersten Junitage stehen im Zeichen der amerikanischen Krebsgesellschaft ASCO und ihrer Jahrestagung in Chicago. Deutsche Biotech-Unternehmen wie Affimed und Apogenix und weitere warten mit aktuellen (prä)klinischen Daten auf, viele davon aus der frühen klinischen Phase. Biontech steuert nach ermutigenden Daten aus einer Phase I/II-Studie schon die zulassungsrelevante Phase III an.







 Morphosys AG
Morphosys AG