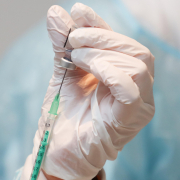
Positive Daten der ARANOTE-Phase III-Zulassungsstudie des Androgenrezeptor-Blockers Darolutamid versprechen der Bayer AG eine milliardenträchtige Indikationserweiterung bei Prostatakrebs.
ANZEIGE
Schlagwortarchiv für: Zulassung
Der Formycon-Konzern hat im ersten Quartal 2024 Umsatzerlöse in Höhe von 17,7 Mio. Euro (Q1/2023: 32,4 Mio. Euro) erwirtschaftet. Diese liegen unter dem Vorjahreswert, bewegen sich aber im Rahmen der Planung, da es im vergangenen Jahr auch eine Sonderzahlung gegeben habe. Die Biosimilarentwickler aus Martinsried bei München haben Produkte auf dem Markt und weitere in fortgeschrittener Phase, sehen sich für die Zukunft gut gerüstet und wünschen sich mehr Verständnis für den hochkompetitiven, aber attraktiven Sektor.
Ein neuer Service hilft Medizintechnikunternehmen herauszufinden, welche Prüfungen zur Biokompatibilität für eine Zulassung ihres Produktes verpflichtend sind. Der BioCompFinder wurde am Naturwissenschaftlichen und Medizinischen Institut (NMI) der Universität Tübingen entwickelt.
Die in München ansässige FGK Clinical Research GmbH erwirbt die britische Clinicology Ltd. und erweitert damit ihre territoriale Präsenz in Europa über den EMA-Zulassungsraum hinaus
Das an der Nasdaq notierte Biotech-Unternehmen CRISPR Therapeutics (Zug, Schweiz) hat mit seinem Partner Vertex Pharmaceuticals nach der Zulassung im Vereinigten Königreich auch von der US-amerikanischen Gesundheitsbehörde FDA die Zulassung für die Gentherapie Casgevy erhalten.
Die österreichisch-französische Valneva SE hat von der US-amerikanischen FDA die weltweit erste Zulassung für einen Impfstoff gegen das Chikungunya-Virus erhalten: für den Lebendimpfstoff IXCHIQ® bei Personen ab 18 Jahren. Die FDA entschied im beschleunigten Zulassungsverfahren (FDA „accelerated approval“) und koppelt dies an weitere konfirmatorische Studien.
BioNTech und OncoC4 haben heute mit der Dosierung des ersten Patienten die zulassungsrelevante Phase III-Studie des BNT316/ONC-392-Programms bei metastasiertem, nicht-kleinzelligem Lungenkarzinom gestartet. Dafür hatte die FDA Ende 2022 den Fast-Track-Status erteilt. Nun soll die randomisierte Phase III-Studie rund 600 Patienten umfassen und in den Vereinigten Staaten beginnen. Anschließend wird sie auf Europa und andere Länder und Regionen ausgeweitet.
Die Insolvenz in Eigenverantwortung hat die ehemalige CO.DON AG nun mit Hilfe eines Investors, der den Geschäftsbetrieb des Leipziger Biopharmazieunternehmens mit weiterem Standort im brandenburgischen Teltow übernommen hat, erfolgreich abgeschlossen. Die meisten Arbeitsplätze bleiben erhalten, nur die ehemaligen Aktionäre haben von zukünftigen Entwicklungen nichts mehr.
Die Notfallzulassung basiert auf klinischen und präklinischen Daten sowie Daten zur Herstellung von an Omikron angepassten bivalenten Impfstoffen. Der bivalente Omikron BA.4/BA.5-Impfstoff enthält 15 µg mRNA, die für das Spike-Protein des Wildtyps von SARS-CoV-2 kodiert sowie 15 µg mRNA, die für das Spike-Protein der Omikron-Subvarianten BA.4/BA.5 kodiert. Der bivalente Omikron BA.4/BA.5-Impfstoff von Pfizer und BioNTech steht zur sofortigen Auslieferung bereit.
Das biopharmazeutische Unternehmen aus dem Bereich der regenerativen Medizin mit Standorten in Leipzig und Teltow in Brandenburg hat beim Amtsgericht Leipzig Antrag auf Eröffnung eines vorläufigen Insolvenzverfahrens in Eigenverwaltung gestellt, um sich in diesem geordneten, gerichtlichen Verfahren zu restrukturieren. Das Gericht hat dem nun zugestimmt.


 Bayer AG
Bayer AG Formycon AG
Formycon AG istockphoto.com/marvinh
istockphoto.com/marvinh Bundesverband Medizinischer Auftragsinstitute (BVMA) e.V.
Bundesverband Medizinischer Auftragsinstitute (BVMA) e.V.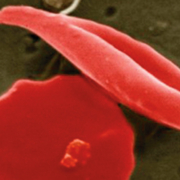 © wikipedia.org/EM Unit, UCL Medical School, Royal Free Campus, Wellcome Images, CC 2.0
© wikipedia.org/EM Unit, UCL Medical School, Royal Free Campus, Wellcome Images, CC 2.0 Valneva SE
Valneva SE