Die Teilnehmer der diesjährigen SLAS Europe im Vienna Congress & Convention Center können sich unter anderem auf wissenschaftliche Sessions, Produktpräsentationen, Networking-Events und einen Blick hinter die Kulissen der Technologie-Anbieter im Vienna BioCenter freuen.
Das diesjährige Programm konzentriert sich auf die drei wichtigsten Bildungsbereiche der Society for Laboratory Automation and Screening – SLAS: Fortschritte in der Arzneimittelforschung, in der Laborautomatisierung sowie Screening-Anwendungen und Diagnostik.

 Viecon, FRBMedia
Viecon, FRBMedia BIO Deutschland
BIO Deutschland BRAIN Biotech AG
BRAIN Biotech AG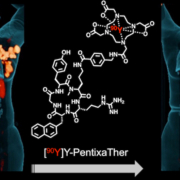 by the Society of Nuclear Medicine (Buck AK, Grigoleit GU, Kraus SK, Schirbel A, Heinsch M, Dreher N, Higuchi T, Lapa C, Hänscheid H, Samnick S, Einsele H, Serfling SE, Werner RA. C-X-C Motif Chemokine Receptor 4-Targeted Radioligand Therapy in Patients with Advanced T-Cell Lymphoma. J Nucl Med. 2022), Uniklinikum Würzburg
by the Society of Nuclear Medicine (Buck AK, Grigoleit GU, Kraus SK, Schirbel A, Heinsch M, Dreher N, Higuchi T, Lapa C, Hänscheid H, Samnick S, Einsele H, Serfling SE, Werner RA. C-X-C Motif Chemokine Receptor 4-Targeted Radioligand Therapy in Patients with Advanced T-Cell Lymphoma. J Nucl Med. 2022), Uniklinikum Würzburg Beiersdorf AG
Beiersdorf AG